ラボラトリーズ
医学の研究と数学
2017年02月20日
真部淳
まなべあつし
聖路加国際病院 小児科
はじめに
私は小児科医である。小児がんの患者は多くない。1年に日本でがんを発症する小児は2000-2500人にすぎない。小児がんの3分の1以上は白血病である。化学療法の進歩により、小児の白血病の予後は過去40年間に劇的に改善し、今では80%以上の患者が治癒するようになった。私自身の話をすると、高校時代まで数学は面白く、「私もいつか、人類の生み出したもっとも高級、高尚な領域である数学に関わって生きていきたい」などとうそぶいていたものである。ところが、大学に入るや、突然、数学がわからなくなった。イプシロンやシータの意味が不明で、早々に数学の世界から脱落してしまった。切ない思い出である。今回は、そのような私が、今、小児がんの臨床研究において数学のお世話になっていることを書いてみたい。
小児白血病の頻度
小児の白血病は少ない。1年間に日本で白血病を発症する小児は600-800人である。日本の15歳未満の小児人口は1605万人(平成28年総務省)であるので、2万人から3万人に1人の小児が白血病を発症することになる。このように発症頻度が低いと、成人のがんのように原因を探ることは難しく、また予防も困難である。
そうはいっても、白血病のようなインパクトの高い病気であるから、古来多くの研究者が原因を探ってきた。まず、白血病を多発する家系はきわめて少ないことがわかっている。ほとんどの場合、白血病に遺伝はないと考えられてきた。また、感染症のようにヒトからヒトにうつる病気でもない。白血病を発症した患者の住所を調べても特に多い地区はない。偶然、その子が白血病を発症するようにみえる。しかし、毎年同じ頻度で発症するのである。ここに近年GWAS(genome-wide association study:ゲノム関連解析)という新たな手法が開発された。
ゲノム解析とはなにか
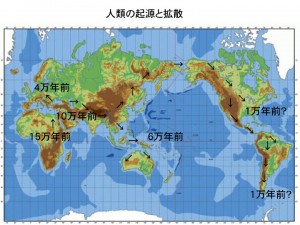
ヒトの細胞には核がある。核は46本の染色体を持ち、デオキシリボ核酸(DNA)という鎖状の分子を有する。DNAはアデニン(A)、チミン(T)、グアニン(G)、シトシン(C)という4つの塩基を持つ。ヒトのゲノム(遺伝子の総体)はおよそ30億のDNAの塩基対から成る。ヒトの遺伝子は約21000ある。DNAの配列は親から子に代々引き継がれてきた。人類は約20万年前にアフリカで誕生したといわれる。その後、ヨーロッパへ、あるいはアジアに移り、最終的にはベーリング海を経て北アメリカ、ついで南アメリカに至ったとされる(図1)。この間、遺伝子は親子代々引き継がれてきたが、その間に染色体の組換えが起こり、全ゲノムのDNAの塩基配列には驚くべき多様性が生じた。一人一人の顔が異なるように、DNAの塩基配列も異なる。21000ある遺伝子の塩基配列は一人一人少しずつ異なっている。たとえば、ある遺伝子の特定の部位の塩基が異なっている(多くの人はAだが少数はGである、多くの人はCだが少数はTである、など)ことがわかってきた。これを1塩基多型(SNP: single nucleotide polymorphism)と呼ぶ。
今、仮に30億の塩基配列のうちSNPを起こしやすい部位50万箇所を選んでみる。ある疾患を発症した患者と発症していない人(正常コントロールという)からDNAを採取し、50万箇所のSNPに違いがあるかどうかを統計的に比較するというのが、GWASのアイデアである。以下に急性リンパ性白血病(小児の白血病に70%を占める)について、今までにGWASを用いてわかった遺伝子を示す:ARID5B(遺伝子), 907(標本数N), Odds比(95% CI)1.65(1.54-1.76), p値:6.7 x 10-19(以下同様); IKZF1, 907, 1.69 (1.58-1.81), 1.2 x 10-19; CEBPE, 907, 1.34 (1.22-1.45), 2.9 x 10-7; PIP4K2A, 2450, 1.40 (1.28-1.53), 1.1 x 10-11。よって、これらの遺伝子の内、たとえば、ARID5Bは極めて重要な遺伝子であり、この遺伝子の変異型SNPを有する子どもはそれを持たない子どもに比べて1.65倍白血病になりやすいことがわかった。また、IKZFIも極めて重要な遺伝子であり、この遺伝子の変異型SNPを有する子どもはそれを持たない子どもに比べて1.69倍白血病になりやすいことがわかった。一方、ARID5B、IKZF1に加えて、CEBPE、PIP4K2Aの合計4つの遺伝子すべてにおいて変異型SNPを有する子どもは9倍白血病になりやすいという結果も発表されている。小児白血病は稀な病気であるが、特定の遺伝子に変異型SNPが存在するか否かにより、発症のしやすさが大きく異なるということは重要な事実であり、こうした特定の遺伝子における変異を防ぐことの意義は非常に高いと言える。しかし、まだ予防するレベルにまで至っていないのが現実である。なお、ここに示す遺伝子には、以前から白血病の病態に関わることが知られているものもあれば、今回初めて意義が見出された遺伝子もあり、今後、白血病の診断と治療の開発に寄与する可能性がある。
ところで、この表に示された研究はすべて欧米から発表されたものである。アメリカの研究によると、ARID5Bの変異SNPは黒人では少なく、ヒスパニックでは多く、白人はその中間だという。世界最大の人口をかかえるアジアの状況は不明であった。そこで、筆者の属する東京小児がん研究グループ(TCCSG)では、小児患者570人と正常コントロール2700人からDNAを採取し、ゲノム上の50万箇所のSNPを調べた。その結果、日本人においてもARID5Bの変異SNPは有意に患者群に多かった(OR 1.75、p値:3.7 x 10-17)(2015年アメリカ血液学会で発表)1)。ヒトの子どもに急性リンパ性白血病をひき起こす可能性のある遺伝子変異はアフリカ(黒人)ではほとんどなく、ヨーロッパとアジアで出現し、南北アメリカ大陸(ヒスパニック)では濃縮されていたことになる。すなわち、人類の起源と拡散そのものの歴史が再現されたのであった(図1)。このGWAS研究には日本を代表する生物統計の叡智ともいう人々が関わっている。かなり大きなコンピューターが必要である。私は数学の恩恵を受けながら研究を行っているのである。今後も、数学者と手を携えて子どものがんについての理解を深めることが、最終的には小児がんの予後のいっそうの改善と、将来は予防に役立つと信じて筆を置く。
1)Urayama KY, Manabe A, et al. Genetic susceptibility loci for childhood acute lymphoblastic leukemia among Japanese. Blood 2015;126:3731